Les chercheurs du laboratoire Reik du Babraham Institute de Cambridge ont obtenu d'excellents résultats. En utilisant les quatre facteurs de reprogrammation de Yamanaka (OSKM), ils ont rajeuni épigénétiquement les cellules humaines de 30 ans.
Les expériences précédentes avaient échoué sur un élément. Si l’exposition des cellules humaines aux facteurs Yamanaka les rajeunit, elle induit une pluripotence pour les transformer en cellules souches, leur faisant perdre leur identité cellulaire (et donc leur fonction).
C'est un problème de longue date. Vous devez exposer vos cellules à ces facteurs assez longtemps pour rajeunissement, mais leur permettant de conserver leur identité.

Les facteurs Yamanaka
Il existe quatre facteurs de transcription: Oct4, Sox2, Klf4 et cMyc (OSKM). Leur utilisation crée des cellules iPS de manière fiable, mais peut provoquer des effets indésirables, dont certains peuvent conduire à des cellules cancéreuses.
L'étude de Cambridge sur les cellules humaines
Les chercheurs de cette étude ils ont utilisé une approche qui exposait les cellules à des facteurs de reprogrammation suffisants pour les pousser au-delà de la limite où elles étaient considérées comme des cellules somatiques plutôt que des cellules souches. Juste au-delà. Les fibroblastes qui ont été reprogrammés de cette manière ont conservé suffisamment de leur mémoire cellulaire épigénétique pour redevenir des fibroblastes. Les chercheurs appellent cette nouvelle méthode reprogrammation transitoire en phase de maturation (MPTR).
Excellents résultats et quelques inconvénients
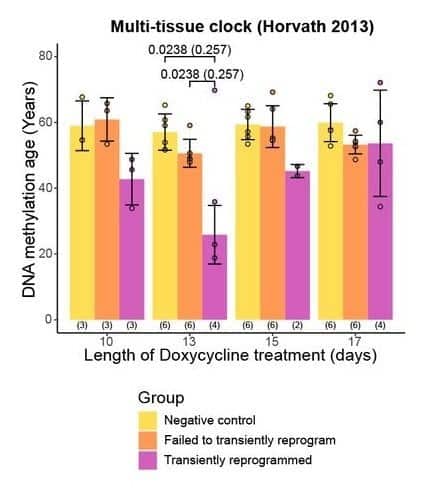
La méthode MPTR a eu des résultats positifs substantiels. Selon l'horloge multi-tissus de Horvath, un test biochimique né en 2013 utilisé pour mesurer l'âge, après 13 jours de reprogrammation, des cellules humaines de 60 ans sont devenues épigénétiquement équivalentes à des cellules âgées d'environ 25 ans. Un autre test né en 2018, l'horloge épigénétique cutanée et sanguine, a montré que des cellules âgées d'environ 40 ans étaient épigénétiquement revenues à celles d'une personne de 25 ans. La technique a également considérablement rajeuni le transcriptome, la collection de protéines produites par les gènes.
Il y a bien sûr quelques mises en garde. Le plus important, bien entendu, est que cette expérience a été réalisée sur des cellules de donneurs humains, mais pas sur un volontaire humain. Par conséquent, les facteurs systémiques connus pour influencer l’épigénome, tels que ceux trouvés dans le sang ancien, n’ont pas été appliqués.
PMTR sur cellules humaines: 10 jours c'est peu, 17 c'est trop long
L'exposition de ces cellules aux facteurs Yamanaka OSKM a également été contrôlée dans les formes posologiques. 10 jours d'exposition n'ont pas rajeuni épigénétiquement les cellules aussi bien que 13 jours d'exposition, mais les chercheurs ont montré qu'une trop grande exposition (15 et 17 jours) entraînait des stress cellulaires qui faisaient vieillir l'épigénome. Cette étude ne portait que sur quelques donneurs et les résultats après 13 jours variaient considérablement d'une personne à l'autre.
L'effet de l'exposition au MPTR sur les télomères
Le MPTR n’a pas influencé positivement le signe de vieillissement de l’attrition des télomères. Lorsque les cellules ont pu être complètement reprogrammées en cellules souches, leurs télomères ont commencé à s’étendre ; mais cette reprogrammation partielle a conduit à un raccourcissement modéré des télomères même s'il a rajeuni les épigénomes des cellules.
De plus, MPTR n’a pas fonctionné sur toutes les cellules humaines et a obtenu ces résultats après des procédures de sélection qui ont divisé les cellules en groupes de reprogrammation ayant échoué et réussi. Cependant, même le groupe « échoué » a obtenu des succès partiels dans de nombreux paramètres clés du vieillissement et de la santé cellulaire.
Conclusions
Bien que cette expérience ait démontré qu'il est possible de reprogrammer épigénétiquement des cellules humaines viables dans des conditions de laboratoire, l'application d'une telle approche en clinique nécessiterait un développement considérable des fondements biotechnologiques afin de fournir à chacune des cellules individuelles du patient la quantité exacte d'OSKM dont il a besoin pour être rajeuni avec succès et pas plus. Cette technologie n’est pas encore à l’horizon.
Et pour les thérapies basées sur des cultures de cellules humaines?
La question est différente quant à savoir si une telle approche peut être utilisée pour le développement de cultures de cellules humaines destinées à être réintroduites chez une personne âgée. Cette expérience a utilisé des fibroblastes, qui forment du collagène. Il est donc raisonnable d’imaginer un monde dans lequel de telles cellules humaines reprogrammées seraient développées comme thérapie contre les rides et autres effets du vieillissement sur la matrice extracellulaire.
Cette approche pourrait un jour être utilisée pour créer des populations viables et rajeunies de cellules musculaires (y compris le muscle cardiaque) et cérébrales. De telles cellules humaines « quasi-somatiques » nouvellement reprogrammées pourraient à terme constituer la meilleure option dans de nombreuses applications cliniques.
Quelle que soit l’approche qui s’avère la plus efficace, nous attendons avec impatience le jour où nos cellules pourront être reprogrammées épigénétiquement chez les jeunes et réintroduites dans notre corps pour conjurer les signes du vieillissement.


